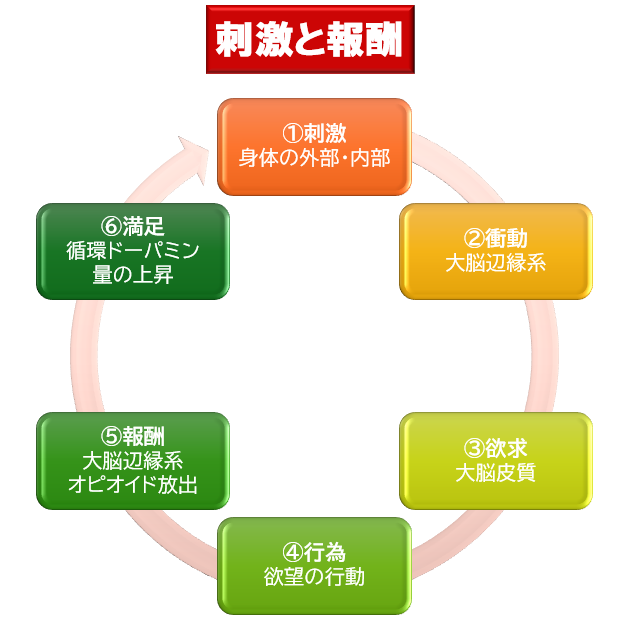
精神疾患の診断や症状に対する効果的な精神療法や薬物療法の探究は、脳の基礎知識が重要となります。
精神疾患は心の問題や症状ではなく、脳の病気とも捉えられます。そのため、治療も薬物や心理・社会的介入、電気的介入などによって脳に働きかける治療を行います。脳を理解することで、精神疾患が理解でき適切な診断や治療を行うことができます。最低限の脳の基礎知識を得ることは、精神疾患の知識を得ることと同等だと考えています。
また、精神疾患の理解には、ゲノムと環境の相互作用についての理解が重要です。遺伝的な要素や環境要因が精神疾患の発症や進行にどのように関与するかを理解することで、疾患のメカニズムや効果的な治療方法についてより深く探究できます。
脳科学と脳の構造は非常に複雑な器官であり、私たちの行動や感情、認知機能などのさまざまな機能を制御していますが、脳の中には神経細胞(ニューロン)があり、これらのニューロンが相互に結合し、電気信号や化学信号を通じて情報を伝達しています。脳は複数の領域に分かれており、それぞれが特定の機能を担当しています。例えば、前頭前野は意思決定や思考に関与し、海馬は学習や記憶に関連しています。
脳の構造や機能を理解するためには、脳の解剖学や神経回路の研究、さらには画像診断技術などが活用されます。近年では、脳活動を測定するための非侵襲的な方法として、脳波計測や機能的磁気共鳴画像法(fMRI)などが広く使われています。
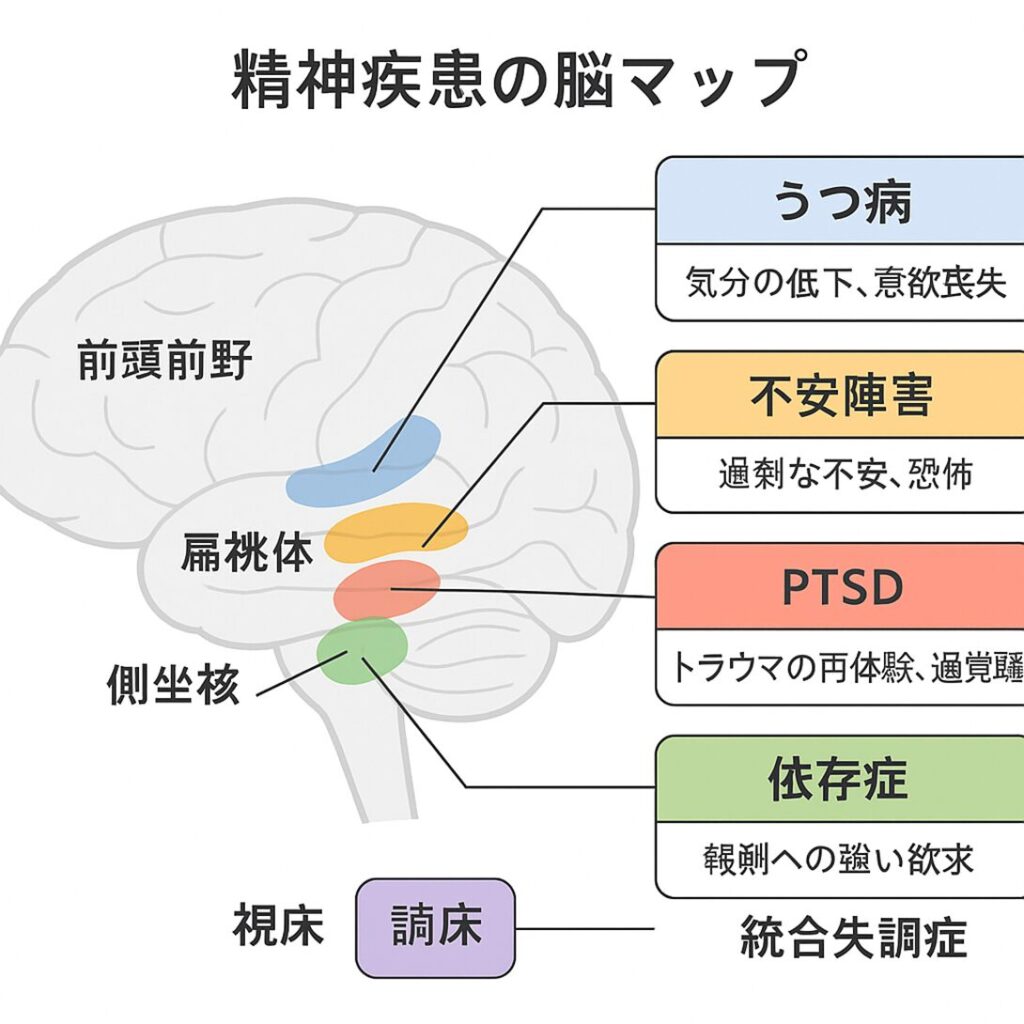
精神疾患と関連する脳の領域・構造と神経伝達物質の要約
精神疾患は「心の病」ではなく、脳の機能異常と密接に関連しています。前頭前野、扁桃体、海馬などの脳領域、ドーパミンやセロトニンなどの神経伝達物質、遺伝と環境要因の相互作用が、それぞれの疾患の発症や症状の現れ方に関与しています。近年の脳科学や遺伝学の進歩により、精神疾患のメカニズムが徐々に解明されつつあり、新しい治療法の開発も進んでいます。
精神疾患と関連する脳の構造
前頭前野は、思考、計画、意思決定、社会的行動の制御などを担う領域です。
前頭前野は精神疾患の「ハブ」とも言える重要部位であり、その活動低下または過活動、ネットワーク異常が精神症状の核心に関与しています。特にDLPFCとvmPFCは多くの疾患で共通して異常が見られ、診断・治療の鍵となります。
■ 前頭前野と関連する主な精神疾患
1. うつ病(Major Depressive Disorder, MDD)
- 異常部位:背外側前頭前野(DLPFC)、腹内側前頭前野(vmPFC)、前部帯状皮質(ACC)との連携部分。
- 特徴:灰白質の減少や血流の低下が見られ、感情の制御や自己評価に関する障害が生じる。
- 臨床的影響:思考のネガティブ化、無気力、意思決定の困難など。
2. 統合失調症(Schizophrenia)
- 異常部位:特にDLPFCの機能不全。
- 特徴:「前頭葉機能低下仮説(hypofrontality)」と呼ばれ、認知機能(作業記憶、注意)の低下が特徴。
- 臨床的影響:思考のまとまりのなさ、実行機能障害、幻覚や妄想への脆弱性。
3. ADHD(注意欠如・多動症)
- 異常部位:DLPFCおよび腹側前頭前野(VLPFC)、ACCとの接続も重要。
- 特徴:前頭前野の発達の遅れや活動の低下が報告されている。
- 臨床的影響:注意持続の困難、衝動的行動、時間感覚の歪みなど。
4. PTSD(心的外傷後ストレス障害)
- 異常部位:vmPFCと扁桃体の連携不全。
- 特徴:vmPFCの機能低下により、扁桃体の過剰な恐怖反応を抑制できなくなる。
- 臨床的影響:過覚醒、フラッシュバック、感情制御困難など。
5. 双極性障害(Bipolar Disorder)
- 異常部位:DLPFC、vmPFC、前帯状皮質など。
- 特徴:躁状態では前頭前野の活動過剰、抑うつ状態では活動低下。
- 臨床的影響:気分の変動、判断力の不安定さ。
■ 前頭前野の機能的区分と精神疾患の関係
| 機能領域 | 主な役割 | 関連疾患 | 影響 |
| DLPFC(背外側) | 注意、作業記憶、意思決定 | うつ、統合失調症、ADHD | 認知の低下、集中困難 |
| VLPFC(腹外側) | 衝動制御、感情の抑制 | ADHD、境界性パーソナリティ障害 | 衝動的行動、怒りのコントロール困難 |
| vmPFC(腹内側) | 感情の統合、自己評価、社会的判断 | PTSD、うつ、双極性障害 | 感情過敏、恐怖制御不能 |
| OFC(眼窩前頭皮質) | 報酬系、社会的行動、嗜癖行動の制御 | 強迫性障害、依存症 | 報酬への過敏、強迫的思考 |
扁桃体は、恐怖や怒り、不安などの情動反応を制御する脳の重要な部位です。
扁桃体(Amygdala)は、情動処理、特に「恐怖」や「不安」の感情に深く関与する脳の辺縁系に属する構造です。小さなアーモンド状の形状で、左右の側頭葉の内側にそれぞれ存在します。
精神疾患との関連では、情動の過敏化、記憶の固定化、社会的認知の障害などに影響し、さまざまな症状の背景にある中核的な構造とされています。
扁桃体は、「恐怖」「不安」など原始的で強い情動に関与し、それが記憶、行動、認知と深く結びついているため、精神疾患の核となる構造の一つです。
とくに、前頭前野や海馬とのネットワークの「バランスの崩れ」が、症状の出現や慢性化に深く関与します。
■ 扁桃体と関連する主な精神疾患
1. PTSD(心的外傷後ストレス障害)
- 扁桃体の状態:過活動が顕著。とくに脅威関連刺激に対して過敏。
- 関連部位:前頭前野(vmPFC)や海馬との制御系のバランスが崩れている。
- 臨床的影響:過覚醒、フラッシュバック、過度な驚愕反応、恐怖の固定化。
2. 不安障害(GAD、社交不安、パニック障害など)
- 扁桃体の状態:持続的に過活動。
- 関連部位:前頭前野との連携不全により、認知的再評価が困難。
- 臨床的影響:危険の誤認識、過剰な心配、回避行動。
3. うつ病(MDD)
- 扁桃体の状態:ネガティブな刺激に対する過敏化、特に初期エピソードで。
- 関連部位:サブジェニュアルACC、vmPFCとの過活動連携。
- 臨床的影響:過去のネガティブ記憶の反芻、悲哀感の強化。
4. 境界性パーソナリティ障害(BPD)
- 扁桃体の状態:情動刺激に対する極端な反応性。
- 臨床的影響:激しい怒り、不安、見捨てられ感、対人関係の不安定さ。
5. 自閉スペクトラム症(ASD)
- 扁桃体の状態:構造の縮小や活動異常が報告されている。
- 臨床的影響:顔の表情からの情動読み取り困難、社会的恐怖の処理異常。
6. 統合失調症(Schizophrenia)
- 扁桃体の状態:構造・機能の異常が見られる(左右の非対称性、縮小)。
- 臨床的影響:感情の平板化、恐怖や怒りの適切な判断困難、妄想の形成への関与。
■ 扁桃体のネットワークと病理
| 扁桃体とのネットワーク | 関連する精神機能 | 精神疾患での異常 |
| vmPFC(腹内側前頭前野) | 恐怖の抑制、感情制御 | PTSD、うつ、不安障害で制御機能低下 |
| 海馬(Hippocampus) | 情動記憶、文脈の記憶化 | PTSDで文脈の誤処理(安全か危険かの判断ミス) |
| 前帯状皮質(ACC) | 情動と認知の統合 | 感情の気づきや抑制が困難に |
| 視床下部 | 自律神経反応(心拍、発汗) | 慢性ストレス反応、身体症状として現れる |
■ 扁桃体の構造異常の研究例
- MRI研究では、扁桃体の体積減少(例:うつ病、ASD)や、機能的MRI(fMRI)での過活動(例:PTSD、不安障害)が多くの研究で報告されています。
- TMSやfMRIニューロフィードバックでは、前頭前野から扁桃体への制御回路を訓練する治療も開発中です。
海馬は、記憶の形成とストレス応答に関与する脳領域です。
海馬(Hippocampus)は、記憶の形成や空間認知、情動の文脈的処理を担う脳の辺縁系に属する重要な構造です。左右の側頭葉の内側に位置し、特に長期記憶の統合と、ストレスに対する調整機能でも中心的な役割を果たします。
精神疾患では、構造的変化(体積の減少)や機能的異常(活動低下・過活動)が多数報告されており、とくに慢性ストレスやトラウマの影響を強く受ける領域です。
海馬は、単なる記憶の中枢ではなく、「いつ・どこで・どう感じたか」という情動的エピソードの記憶の中核であり、それが精神疾患と密接に関わっています。
特に、慢性ストレス、トラウマ、情動の抑制障害がある場合、海馬の機能不全が症状の根底にあることが多いです。
■ 海馬と関連する主な精神疾患
1. PTSD(心的外傷後ストレス障害)
- 状態:海馬の体積減少がしばしば見られる(トラウマ前後での比較研究もあり)。
- 機能障害:出来事の「文脈的処理」がうまくできず、「安全な状況でも危険と誤認」してしまう。
- 臨床的影響:フラッシュバック、時間感覚のゆがみ、現実との切断感(離人症)など。
2. うつ病(Major Depressive Disorder)
- 状態:慢性のうつ病では、海馬体積の縮小が多く報告される(特に未治療の場合)。
- 機能障害:新しい記憶の形成障害、ネガティブ記憶の強化。
- 臨床的影響:集中困難、学習効率低下、過去の記憶の反芻。
3. アルツハイマー型認知症(AD)
- 状態:最初期から海馬が萎縮。早期診断の指標としても重要。
- 機能障害:記憶の保持・再生が困難になり、見当識(時間や場所の感覚)も障害される。
- 臨床的影響:物忘れ、迷子になる、感情の不安定化。
4. 統合失調症(Schizophrenia)
- 状態:海馬の体積減少・異常な神経発火(過活動)が観察される。
- 機能障害:記憶の組織化障害、現実検討機能の低下。
- 臨床的影響:幻覚・妄想への関連(記憶と現実の混同)。
5. 双極性障害(Bipolar Disorder)
- 状態:特に反復エピソードが多いと海馬体積が減少する傾向。
- 機能障害:記憶や気分の変調に影響する可能性。
- 臨床的影響:気分の急変とともに、過去の体験への過剰な執着や空白感が生じる。
■ 海馬の脆弱性とストレスホルモン
- 慢性ストレス下で分泌されるコルチゾール(ストレスホルモン)は、海馬の神経細胞にダメージを与えることがわかっています。
- 長期的な高コルチゾール状態では、神経新生の抑制、シナプス機能の低下、体積減少が起きやすくなります。
- このため、「ストレス―海馬―記憶障害」という病理軸は、PTSDやうつ病の理解にとって非常に重要です。
■ 海馬のネットワーク的役割
| 連携する領域 | 機能 | 精神疾患での障害 |
| 扁桃体 | 情動記憶のタグ付け(恐怖や喜びの記憶) | PTSDで恐怖記憶が文脈と切り離されてフラッシュバック化 |
| 前頭前野(PFC) | 記憶の抑制と統合 | 抑うつ状態で記憶のバランスが崩れ、ネガティブな記憶が優位になる |
| 帯状回(Cingulate Cortex) | 注意と情動の橋渡し | 不安や抑うつで注意が過去に偏る(反芻思考) |
「前頭前野―扁桃体―海馬」の三者ネットワークは、感情の認知、記憶の処理、ストレスへの適応といった心の働きを支える中核的な神経回路です。このネットワークがバランスよく機能しているときは、感情と記憶がうまく統合され、柔軟な対応が可能になります。
しかし、精神疾患ではこのネットワークの連携不全や機能の偏りが見られ、感情の暴走・記憶の誤作動・ストレス過敏などの症状が生じます。
■ 三者のネットワークが意味すること
- 扁桃体:感情の「点火装置」
- 海馬:出来事の「記録係」
- 前頭前野:全体の「司令塔・意味づけ役」
この三者が連携しあうことで、私たちはただ反応するのではなく、「体験として意味ある感情」を形成できます。精神疾患とは、そのつながりの断裂や偏りともいえるのです。
■ 三者それぞれの役割
| 領域 | 主な機能 | 精神的役割 |
| 前頭前野(PFC) | 抑制、意思決定、認知的再評価 | 感情のコントロール、意味づけ |
| 扁桃体(Amygdala) | 恐怖・不安などの情動処理 | 危険の感知、情動の引き金 |
| 海馬(Hippocampus) | エピソード記憶、文脈情報の統合 | 「いつ・どこで・なぜ怖かったか」の記憶化 |
■ 三者のネットワーク構造と相互作用
1. 前頭前野 → 扁桃体:感情の抑制と調整
- 健常時:前頭前野(とくにvmPFCやDLPFC)が扁桃体の過剰反応を抑える。
- 障害時(例:PTSD、BPD、不安障害):前頭前野の制御機能が弱くなり、扁桃体の恐怖反応が暴走。
- 結果:過覚醒・過剰な不安・衝動的行動
2. 扁桃体 → 海馬:情動の強化と記憶のタグ付け
- 健常時:扁桃体が「情動の強さ」を信号として海馬に送り、重要な出来事として記憶される。
- 障害時(例:PTSD):強い恐怖により「情動だけが強く、文脈が欠落した記憶」として保存される。
- 結果:フラッシュバック、感情と現実の切断感
3. 海馬 → 前頭前野:記憶と文脈を提供して判断に寄与
- 健常時:過去の体験や状況の文脈を前頭前野に伝えることで、適切な判断をサポート。
- 障害時(例:うつ病、AD):記憶の文脈化がうまくいかず、判断が極端に(悲観的・混乱的に)なる。
- 結果:反芻思考、未来への予測困難
■ 三者の連携不全による病的サイクル(例:PTSD)
① 外的刺激 → 扁桃体が過剰に反応(恐怖)
⇓
② 海馬が文脈化できず(場所や時間を認識できない)
⇓
③ 前頭前野がうまく制御できない(再評価できない)
⇓
④ 再び扁桃体が過活動(恐怖が再活性化)
→ このサイクルが慢性化し、フラッシュバックや回避行動が持続
■ 臨床的意義:このネットワークが示す治療のターゲット
| 治療法 | 主な作用部位 | 効果 |
| 認知行動療法(CBT) | 前頭前野 | 思考再構成による扁桃体の調整 |
| マインドフルネス・瞑想 | 海馬・前頭前野 | 注意の安定と感情の距離化 |
| EMDR(眼球運動による脱感作) | 海馬・扁桃体 | 情動記憶の再統合 |
| TMS(経頭蓋磁気刺激) | DLPFC(背外側前頭前野) | 前頭前野の活性化による感情制御 |
| 薬物療法(SSRIなど) | 扁桃体・前頭前野 | 不安やうつ症状の緩和、ネットワークの再バランス |
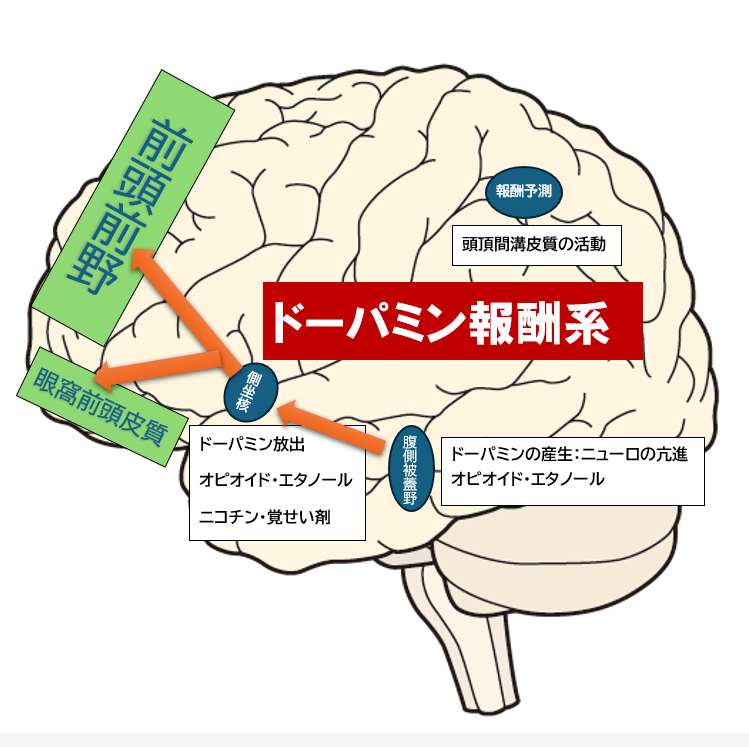
側坐核は、報酬系(快楽やモチベーション)に関与する領域で、ドーパミンの影響を受けます。
精神疾患との関係では、報酬感覚の鈍化・過剰な欲求・快楽の誤作動といった形で多くの病理に関わっています。
■ まとめ:側坐核とは?
- 「快の司令塔」「やる気の火種」
- 適切に働けば、興味・集中・達成感を生むが、過活動・低活動どちらでも精神疾患のリスクになる。
- 「ただ楽しい」ではなく、「報われると感じられる」という報酬の感覚が、心の健やかさの要。
側坐核(Nucleus Accumbens、略称:NAcc)は、「快・報酬・動機づけ・強化学習」を司る中枢的な脳部位で、線条体の一部(腹側線条体)に分類されます。特にドーパミン系との関連が強く、「やる気」や「快の予測」に関与するため、「報酬系のハブ」とも呼ばれます。
■ 側坐核と関連する主な精神疾患
- 1. うつ病(Major Depressive Disorder)
-
- 状態:側坐核のドーパミン活動の低下が見られる。
- 症状との関連:
- 興味の喪失(アネドニア)
- 「やる気が出ない」「楽しめない」感覚
- 臨床的意義:報酬を予測しても快感が生じず、努力する動機がわかず、抑うつが悪循環化。
- 2. 統合失調症(Schizophrenia)
-
- 状態:報酬系の誤作動(過活動・不適切な動機づけ)
- 症状との関連:
- 陽性症状:無関係な刺激にも意味づけをしてしまう(妄想的信念)
- 陰性症状:動機の喪失、快楽の消失
- 臨床的意義:報酬の予測と反応のミスマッチが認知の歪みを形成
- 3. 依存症(薬物・ギャンブル・スマホ依存など)
-
- 状態:快感刺激により側坐核のドーパミン分泌が過剰に起こり、報酬系がハイジャックされる。
- 症状との関連:
- 渇望、耐えられない欲求
- 禁断症状時の無快感(快感のベースライン低下)
- 臨床的意義:報酬系の「過剰な学習」と「報酬の不感症」が共存する病態
- 4. ADHD(注意欠如・多動症)
-
- 状態:側坐核を含む報酬系の反応が低反応または遅延している。
- 症状との関連:
- 短期的な刺激には敏感だが、長期的報酬にモチベーションが続かない。
- 臨床的意義:即時報酬がない活動(勉強、片付け)に取り組むのが困難になる。
- 5. 双極性障害(Bipolar Disorder)
-
- 状態:躁状態では側坐核が過活動、抑うつ状態では活動低下。
- 症状との関連:
- 躁:万能感・快感追求・過剰な自信
- 抑うつ:興味喪失・行動の停止
- 臨床的意義:気分の波と報酬感覚の強弱が連動している。
-

■ 側坐核とドーパミン系ネットワーク
| 経路 | 機能 | 関与する疾患 |
| 腹側被蓋野(VTA)→ 側坐核 | ドーパミンの報酬信号伝達 | 依存症、うつ病 |
| 側坐核 → 前頭前野(PFC) | 報酬の予測に基づいた意思決定 | ADHD、統合失調症 |
| 扁桃体 ↔ 側坐核 | 情動と報酬の連携 | 依存症、双極性障害 |
■ 治療との関連
| 治療法 | 効果の焦点 | 働きかけ |
| SSRI/SNRI | 間接的にドーパミン経路を改善 | 側坐核の活動回復(アネドニア緩和) |
| 刺激制御療法(依存症) | 側坐核の報酬感度を調整 | 快刺激の制限と再学習 |
| 行動活性化療法(うつ病) | 側坐核の快感覚の再訓練 | 少しずつ「できた→気持ちいい」を増やす |
| 報酬遅延トレーニング(ADHD) | 側坐核の報酬待機力の向上 | 「即時報酬」に頼らない習慣化を促す |
視床は、感覚情報の中継を行い、意識や注意、認知機能に関与します。
視床(Thalamus)は、感覚情報や運動情報の中継ステーションとして知られる脳の中心部にある構造で、大脳皮質と脳幹・辺縁系との橋渡し役を担います。ただの「中継点」ではなく、情報の選別・強調・タイミング調整という高度な調整機能を持っており、精神疾患の多くに深く関わります。
■ 視床の基本機能
| 領域 | 主な機能 |
| 視床(Thalamus) | ・感覚入力(嗅覚を除く)を皮質に中継 ・注意の選択的制御 ・睡眠と覚醒の切り替え ・前頭前野、扁桃体、海馬などと連携して「意味のある情報」に編集 |
■ 視床とは?
- 精神のゲートキーパー:「何を現実とし、何を無視するか」を決める中枢。
- 多くの精神疾患で、視床の感覚フィルター機能や認知中継機能の障害が見られる。
- その調整により、現実への関わり方・感情の安定・集中の維持が支えられている。
- 統合失調症:視床の機能異常が知覚障害(幻覚など)や注意のコントロールの問題を引き起こす。
■ 精神疾患との関連
1. 統合失調症(Schizophrenia)
- 状態:視床と前頭前野を結ぶ回路の機能異常(とくにMD核:内側背側核)
- 症状との関係:
- 思考のまとまりのなさ(思考の分裂)
- 感覚のフィルタリング異常(過剰な入力や幻覚)
- 神経画像研究:
- 視床の灰白質減少
- 視床―皮質間の接続性の低下(特に前頭葉)
2. うつ病(Major Depression)
- 状態:視床の活動が過剰または低下(症状により異なる)
- 症状との関係:
- 注意集中の困難(情報の選別ができない)
- 睡眠障害(覚醒と睡眠の切替調節不全)
- 神経画像研究:
- 視床内の活動パターン異常(とくにDLPFCとの接続性低下)
3. ADHD(注意欠如・多動症)
- 状態:視床―皮質ループの発達遅延または機能不全
- 症状との関係:
- 注意の切り替えが困難
- 感覚過敏・衝動的な反応(情報フィルターの不全)
- 研究知見:
- 小児ADHDでは視床が小さく、機能的接続も低下している。
4. PTSD(心的外傷後ストレス障害)
- 状態:感覚刺激の処理と感情回路の協調の乱れ
- 症状との関係:
- フラッシュバック(現在と過去の感覚の混同)
- 脅威に対する過剰な警戒(視床が「過敏化」している)
- 機序の一例:
- 外部刺激 → 扁桃体の過活動 + 視床のフィルター不全 → 現実検討力が弱まる
5. 双極性障害(Bipolar Disorder)
- 状態:気分状態によって視床の活動パターンが変動
- 症状との関係:
- 覚醒・不眠(躁)
- 情報処理の遅延(うつ)
- 脳機能研究:
- 情動刺激に対する視床の反応性が気分によって変わる。
■ 機能別・視床のサブ領域と精神症状の関係
| 視床の部位 | 関連皮質 | 機能 | 関連症状 |
| 内側背側核(MD核) | 前頭前野 | 認知制御・判断 | 統合失調症、うつ病 |
| 後内側腹側核(VPM)/ 外側膝状体(LGN) | 感覚・視覚野 | 感覚処理 | ADHD、PTSD |
| 視床網様核(TRN) | 全体制御 | 注意の選択・抑制 | 感覚過敏、不安障害 |
| 前核群(ANT) | 海馬系 | 記憶、空間認知 | 認知症、PTSD |
■ 視床が果たす「精神的意味」の側面
- 視床は「心のセンサーゲート」:何を見て、何を無視するかを決める装置。
- そのフィルターが壊れると、過剰な世界(幻覚・混乱)や、鈍く冷たい世界(うつ・感情鈍麻)が立ち現れる。
- 言い換えれば、視床は「現実の編集者」。編集が乱れると、物語が支離滅裂になる。
■ 治療的な示唆
| アプローチ | 狙い | 方法 |
| マインドフルネス瞑想 | 視床の注意制御を回復 | 刺激に反応せず、観察する練習 |
| CBT | 認知情報の再選別 | 視床―前頭前野の連携改善 |
| TMS(経頭蓋磁気刺激) | 視床―前頭皮質ループの調整 | うつ・統合失調症への介入 |
| 薬物療法(抗精神病薬など) | 異常な視床活動の抑制 | ドーパミン経路やNMDA受容体への作用 |
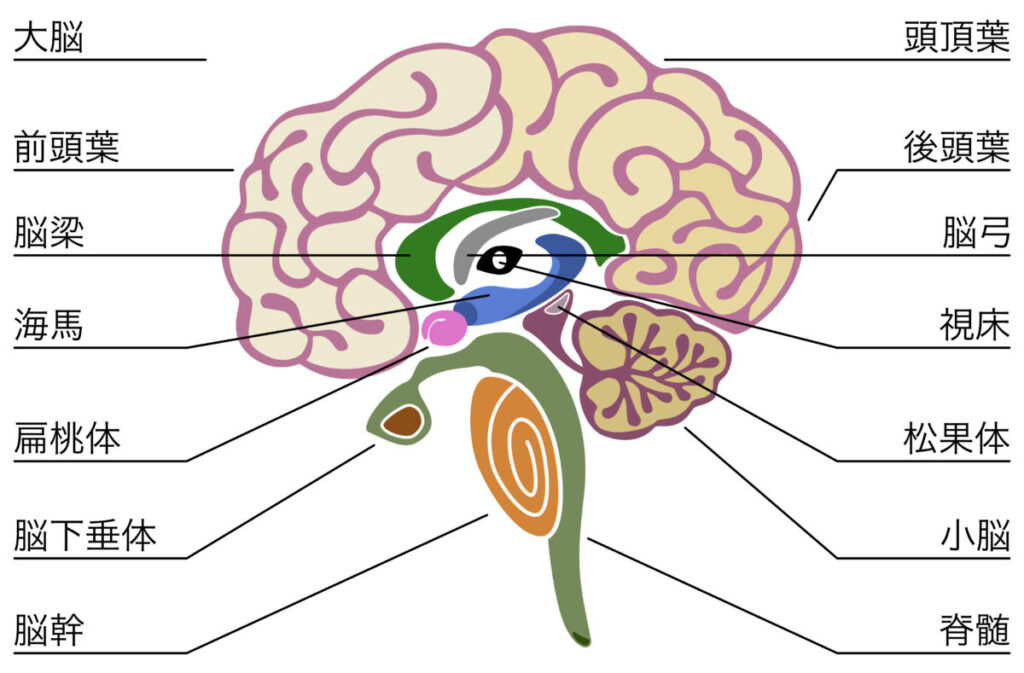
5つの主要部位以外に注目すべき脳領域
5つの主要部位(前頭前野・扁桃体・海馬・側坐核・視床)は、精神疾患における中核的ネットワークを構成していますが、これらに加えて注目すべき脳構造を扱うには、「ネットワーク全体でどのように異常が広がるのか?」という視点が重要になります。
■ 追加で注目すべき脳構造と精神疾患
1. 帯状回(Cingulate Gyrus)
- 特に前部帯状回(ACC)は、情動と認知の統合を担う。
- 【関連疾患】うつ病、統合失調症、強迫性障害、ADHD
- 【臨床的意義】感情と行動をつなぐハブ。葛藤処理や「間違いに気づく」働き。
2. 島皮質(Insula, 内側脳)
- 身体感覚と感情の結びつき(内受容感覚)を担う。
- 【関連疾患】不安障害、PTSD、解離性障害、摂食障害
- 【臨床的意義】「感じすぎる」または「感じない」自己感覚の障害がここに関係。
3. 小脳(Cerebellum)
- 運動だけでなく、感情や認知のタイミング調整・予測に関与。
- 【関連疾患】統合失調症、自閉スペクトラム症(ASD)、双極性障害
- 【臨床的意義】「心のリズム感」や予測制御の障害と関係。
4. 脳幹(特に青斑核、縫線核)
- ノルアドレナリン・セロトニンなどの原発部位で、覚醒・不安・気分を制御。
- 【関連疾患】うつ病、PTSD、パニック障害、ASD
- 【臨床的意義】薬物療法がここを主にターゲットとしている。
5. 側頭極・側頭葉前部(Anterior Temporal Lobe)
- 自伝的記憶、他者理解、社会的知覚に関わる。
- 【関連疾患】自閉スペクトラム症、反社会的人格障害、認知症
- 【臨床的意義】「他者を人間として感じる力」に影響。
■ 解釈の枠組み:ネットワーク思考のすすめ
精神疾患と脳構造の関係は、個々の部位を見るだけでなく、「ネットワークの連携障害としてとらえる」視点が有効です。
◎ 3つの主要ネットワーク(近年の神経科学に基づく枠組み)
| ネットワーク名 | 主な構成 | 役割 | 関連疾患 |
| DMN(デフォルトモードネットワーク) | 海馬・内側前頭前野・後部帯状回など | 内省・自伝的記憶・未来想像 | うつ、PTSD、ASD |
| SN(サリエンスネットワーク) | 島皮質・扁桃体・前部帯状回など | 注意の切替・意味づけ | パニック障害、統合失調症 |
| CEN(中央実行系ネットワーク) | 背外側前頭前野・頭頂葉 | 認知制御・問題解決 | ADHD、認知症、うつ |
精神疾患ごとの脳マップ一覧(簡易表)
各疾患の「主症状」と「関与部位」「ネットワーク異常」「臨床的含意(意味)」が視覚的に整理できるように一覧にしています。
■ 精神疾患ごとの脳マップ一覧(簡易表)
| 精神疾患 | 主な症状 | 主に関与する脳構造 | ネットワーク異常 | 臨床的含意 |
| うつ病(MDD) | 気分の低下、意欲喪失、罪悪感 | 前頭前野(DLPFC)、扁桃体、視床、帯状回、海馬 | DMN ↑、CEN ↓、サリエンス ↓ | ネガティブ思考のループ、感情調整失敗、記憶の固定化 |
| 統合失調症 | 妄想、幻覚、思考の脱線 | 前頭前野、視床、海馬、小脳、側頭葉 | DMN/CENの分離障害、サリエンス誤作動 | 「意味」の異常検出、現実検討力の低下、時間認知のゆがみ |
| PTSD | フラッシュバック、過覚醒、回避 | 扁桃体↑、海馬↓、前帯状回、島皮質、視床 | サリエンス ↑、DMNの崩壊 | 脅威記憶の固定、現在―過去の混同、身体感覚の過敏化 |
| ADHD | 注意散漫、衝動性、多動 | 前頭前野(特に右DLPFC)、帯状回、視床、側坐核 | CEN ↓、サリエンス ↓ | 注意制御・報酬予測の失敗、感覚選択の困難 |
| 自閉スペクトラム症(ASD) | 社会的相互作用困難、感覚過敏、こだわり | 扁桃体、側頭極、島皮質、小脳、前頭前野 | DMN・サリエンスの接続不良 | 他者の心の理解(心の理論)や感情共鳴の困難 |
| 双極性障害(躁うつ病) | 気分の波、衝動、睡眠障害 | 側坐核、扁桃体、前頭前野、帯状回 | サリエンス・報酬系の過活動/低下 | 感情調整のブレ、快感追求と抑制の不均衡 |
| 強迫性障害(OCD) | 強迫観念・行動、安心感への固執 | 前頭眼窩皮質(OFC)、前帯状回、尾状核 | CEN ↑、DMN ↓、皮質―線条体回路の過活動 | 不安解消行動の強化、意味づけの異常、抑制困難 |
| 摂食障害(拒食/過食) | 身体イメージの歪み、食行動の異常 | 島皮質、扁桃体、海馬、前頭前野 | DMN過活動、体内感覚系異常 | 自己感覚と身体感覚の乖離、制御不能感 |
■ 用語の補足(ネットワーク)
- DMN(デフォルトモードネットワーク):内省・自己関連思考・過去未来想起
- CEN(中央実行系ネットワーク):注意・計画・意思決定などの実行機能
- サリエンスネットワーク(SN):刺激の重要性の検出・注意の切替
- 皮質―線条体―視床ループ:行動の制御や反復的行動との関連が強い(OCDなど)
- 「このクライエントは どの回路(感情・記憶・報酬・認知)に偏りがあるか?」
- 「症状は過剰な活動か?低下か?それとも調整の失敗か?」
- 「脳構造を単体でなく協奏するシステムとしてとらえることが、理解と支援の鍵」
■ 臨床的なまとめ:どう使って考えるか?
精神疾患と関連する神経伝達物質の異常
- 統合失調症:ドーパミンの過剰活動(特に側坐核)が陽性症状(幻覚・妄想)に関連。一方で、前頭前野のドーパミン不足が陰性症状(意欲低下、感情鈍麻)と関連。
- パーキンソン病:黒質ドーパミン神経の喪失が運動障害を引き起こすが、精神症状(うつ、不安、幻覚)にも関与。
- うつ病:セロトニンの不足が抑うつ気分、不安感、自殺念慮と関連。SSRI(選択的セロトニン再取り込み阻害薬)が抗うつ薬として有効。
- 強迫性障害(OCD):セロトニン系の異常が強迫観念・強迫行動の原因の一つとされる。
- うつ病:ノルアドレナリンの不足がエネルギー低下や興味喪失と関連。
- PTSD:ノルアドレナリンの過活動が過覚醒状態を引き起こす。
- 統合失調症:グルタミン酸の機能低下(特にNMDA受容体の機能異常)が認知機能の障害と関連。
- 双極性障害:グルタミン酸の過剰活動が躁状態の原因の一つと考えられる。
- 不安障害:GABAの不足が不安感や過覚醒を引き起こす。ベンゾジアゼピン系薬(抗不安薬)はGABAの作用を強める。
- 統合失調症:GABAの低下が認知機能の低下や幻覚・妄想に関与。
遺伝と環境の相互作用
精神疾患の多くは遺伝要因と環境要因が相互作用して発症することが多くあります。
- 統合失調症や双極性障害は高度な遺伝性がある(家族に同じ疾患があると発症リスクが高まる)。
- ゲノムワイド関連解析(GWAS)によって、多くの精神疾患に関連する遺伝子多型が発見されている。
- 幼少期のトラウマやストレス(虐待、ネグレクト)が精神疾患の発症リスクを高める。
- 妊娠中の栄養状態やウイルス感染(母親の風疹感染など)が胎児の脳発達に影響を与える可能性がある。
- 都市部での生活や社会的ストレスも精神疾患のリスク因子。